Jak HNO3 reaguje s nekovy
Jestli kyselina dusičná reaguje s nekovy, to obecně lze
říci, že produkty rekce budou:
1. Nekov se oxiduje do svého nejvyššího oxidačního čísla (odpovídá číslu skupiny periodické tabulky, v které se nekov
nachází) a tvoři přitom kyselinu.
Příklad. S0 se oxiduje kyselinou dusičnou do SVI a produktem reakci bude H2SVIO4.
2. Produkt redukce HNO3:
| HNO3 |
Produkt redukce HNO3 |
| zředěná |
NO |
| koncentrovaná |
NO2 |
Poznámka:
V tomto typu reakci voda nemusí byt zapsána vůbec, může byt v levé nebo v pravé části rovnice. Proto se doporučuje
začít upravovat reakci a vodu zapsat do té části rovnice, kde budou chybět vodík a kyslík.
Příklad 1.
2HNO3 zředěná + S = H2SO4 + 2NO
NV + 3e = NII | 6 | 2
S0 - 6e = SVI | 3 | 1
| redukce | : | NV 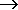 NII NII |
| oxidace | : |
S0 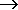 SVI SVI |
| redukční činidlo | : | S |
| oxidační činidlo | : | HNO3 |
Příklad 2.
4HNO3 koncentrovaná + C = H2CO3 + 4NO2 + H2O
NV + 1e = NIV | 4
C0 - 4e = SIV | 1
| redukce | : | NV 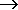 NIV NIV |
| oxidace | : |
C0 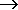 CIV CIV |
| redukční činidlo | : | C |
| oxidační činidlo | : | HNO3 |
Příklad 3.
5HNO3 zředěná + 3P + 2H2O = 3H3PO4 + 5NO
NV + 3e = NII | 5
P0 - 5e = PV | 3
| redukce | : | NV 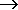 NII NII |
| oxidace | : | P0 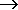 PV PV |
| redukční činidlo | : | P |
| oxidační činidlo | : | HNO3 |
Příklad 4.
5HNO3 koncentrovaná + As = H3AsO4 + 5NO2 + H2O
NV + 1e = NIV | 5
As0 - 5e = AsV | 1
| redukce | : | NV 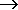 NIV NIV |
| oxidace | : |
As0 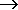 AsV AsV |
| redukční činidlo | : | As |
| oxidační činidlo | : | HNO3 |


