Redoxní reakce - rozdělení
Redoxní reakce mužeme rozdělit podle počtu atomů, které během reakce mění svá oxidační čísla.
1. Atomy dvou prvků mění svá oxidační čísla
2KMnO4 + 5Na2SO3 + 3H2SO4 = 2MnSO4 + 5Na2SO4 + K2SO4 + 3H2O
MnVII + 5e = MnII | 2
SIV - 2e = SVI | 5
| redukce |
: |
MnVII 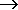 MnII
MnII |
| oxidace |
: |
SIV 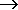 SVI
SVI |
| redukční činidlo |
: |
Na2SO3 |
| oxidační činidlo |
: |
KMnO4 |
2. Atomy jednoho prvku mění své oxidační čislo
a) 3Cl2 + 6KOH = 5KCl + KClO3 + 3H2O
Cl20 + 2e = 2Cl-I 10 | 5
Cl20 - 10e = 2ClV 2 | 1
| redukce |
: |
Cl20 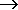 2Cl-I 2Cl-I |
| oxidace |
: |
Cl20 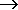 2ClV 2ClV |
| redukční činidlo |
: |
část molekul Cl20 |
| oxidační činidlo |
: |
část molekul Cl20 |
b) KBrO3 + 5KBr + 3H2SO4 = 3Br2 + 3K2SO4 + 3H2O
Br+V - 5e = Br0 | 1
Br-I + 1e = Br0 | 5
| redukce |
: |
Br+V  Br0
Br0 |
| oxidace |
: |
Br-I  Br0
Br0 |
| redukční činidlo |
: |
KBr |
| oxidační činidlo |
: |
KBrO3 |
3. Atomy tří prvků mění svá oxidační čísla
10FeCl2 + 6KMnO4 + 24H2SO4 = 5Fe2(SO4)3 + 10Cl2 + 6MnSO4 + 3K2SO4 + 24H2O
FeII - 1e = FeIII
2Cl-I - 2e = Cl20
MnVII + 5e = MnII
Sečteme množství elektronů, které odevzdává molekula FeCl2, to jest 1 atom FeII a 2 atomy Cl-I, součet zapíšeme jako koeficient pro mangan. Vzhledem k tomu, že v pravé části rovnice nemůžeme zapsat pět atomů železa (měli bychom zapsat koef. 2,5, což se nepoužívá), oba koeficienty vynásobíme dvěma.
FeII - 1e = FeIII \
5 x 2 = 10
2Cl-I - 2e = Cl20 /
MnVII + 5e = MnII - 3 x 2 = 6
| redukce |
: |
MnVII  MnII
MnII |
| oxidace |
: |
FeII  FeIII,
FeIII,
2Cl-I  Cl20 Cl20 |
| redukční činidlo |
: |
FeCl2 |
| oxidační činidlo |
: |
KMnO4 |


